一、背景
二、靶向药物与131I联合治疗模式探索
01. 特异性靶向药物逆转病灶碘摄取能力(潜在作用机制及现有研究数据)
02. 泛靶点靶向药物助力131I治疗(潜在作用机制及现有研究数据)
三、总结与展望
根据世界卫生组织国际癌症研究机构的GLOBOCAN 2020癌症发病率和死亡数据库,甲状腺癌是全球第九高的癌症发病率1, 2。尽管甲状腺癌可以发生在任何性别的人群中,但女性约占所有甲状腺癌患者的75%3。甲状腺癌可以发生在不同年龄段,但诊断的中位年龄为50多岁。甲状腺癌是16至33岁青少年和成年人中最常见的恶性肿瘤4。
甲状腺癌分为三个主要类型:分化型甲状腺癌(DTC,包括乳头状、滤泡状和嗜酸性细胞状甲状腺癌)、甲状腺髓样癌(MTC)和未分化型甲状腺癌(ATC,通常由分化型甲状腺癌演变而来,具有较高的死亡率)。虽然各国的癌症类型分布可能有所不同,但乳头状甲状腺癌约占80%的病例5。
在过去的5到10年里,甲状腺癌的治疗已经发生了变革,不断有新的治疗选择出现。局部晚期或转移性甲状腺癌是甲状腺癌患者死亡的重要原因。近年来不断涌现的靶向药物为晚期甲状腺癌的治疗提供了更多治疗选择,显示出良好的治疗效果,也是提高患者生存时间及质量的重要手段6。
对于可切除的复发、转移性DTC与MTC,手术是整体治疗方案的首选。需要注意的是,若复发/转移的 DTC 病灶仍保留良好摄碘功能,放射性碘治疗(RAI)仍是术后常规治疗手段之一,可能缓解病情或有临床治愈的价值7。
分化型甲状腺癌通常可以通过手术和RAI治疗(约85%)进行治疗。然而,60%的侵袭性转移性DTC患者对RAI治疗产生抵抗,并且整体预后较差。若RAI疗效不佳,即呈现为碘难治(RAI refractory,RAIR)状态(出 现 下 列 情 形 之 一 即 可 界 定 为 RAIR:①病灶在131I治疗后全身显像上表现为不摄碘,且无法从后续的131I 治疗中获益(如残留甲状腺太多,可能会影响转移灶摄碘,可清甲后再次治疗时进行评估);②原本摄碘的病灶经131I 治疗后逐渐丧失摄碘能力;③同一患者体内部分病灶摄碘,而部分病灶不摄碘,且生化无缓解;④病灶摄碘,但在1 年内出现疾病进展;⑤131I累积用量超过 600 mCi,但疾病无缓解。)8,9,则不应继续进行RAI治疗。对常规治疗无效、临床证据呈明显进展或有肿瘤进展相关症状的全身或局部晚期甲状腺癌,应考虑行靶向药物治疗。
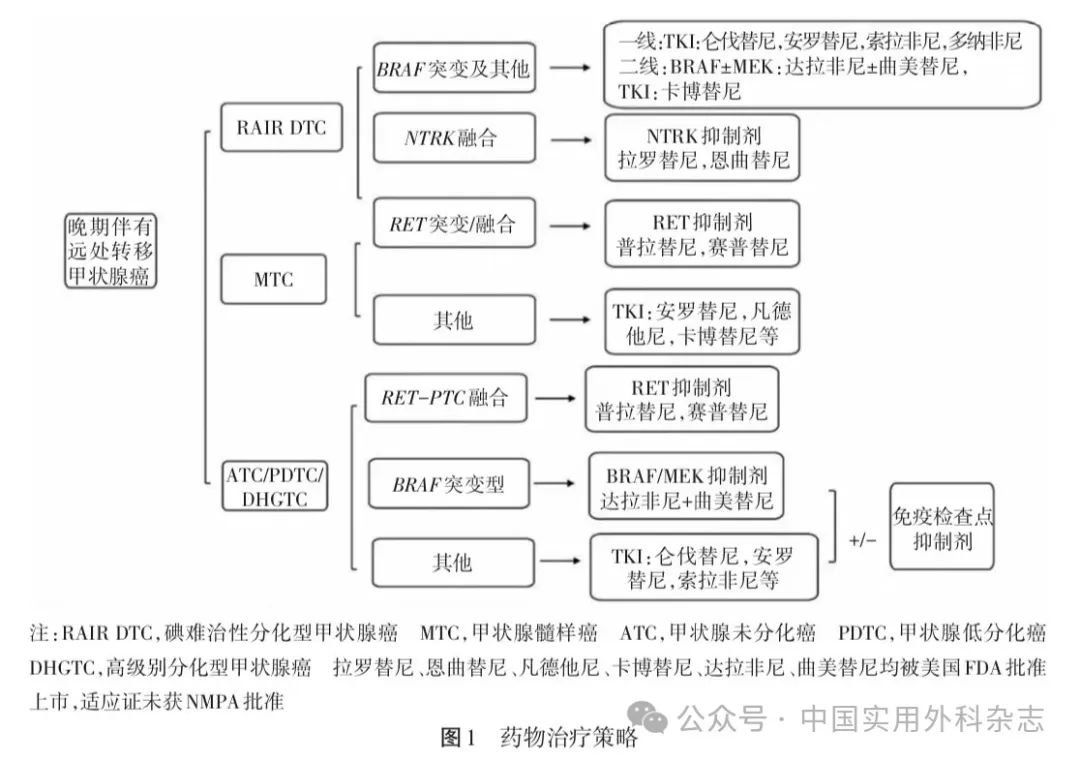
目前甲状腺癌靶向治疗药物分为泛靶点的多激酶抑制剂,以及特异性靶向药物——高度选择性抑制剂两类。相关药物推荐如下6:

那么,靶向药物在甲状腺癌治疗中是否仅适用于碘难治型甲状腺癌,靶向药物与放射性碘治疗是否存在新的联合治疗潜力,以为患者提供更大的临床效益?本文对此问题进行探讨。
①潜在作用机制——DTC细胞重获摄碘能力
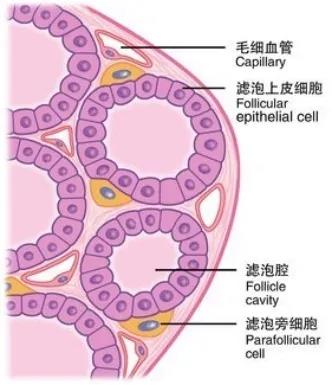
在过去几十年中,对于导致分化型甲状腺癌恶性演变和放射性碘抗药性转变的分子机制研究取得了显著进展。在生理条件下,碘可以特异性地积聚在甲状腺组织中,这归因于位于甲状腺细胞基底侧膜上的钠碘共转运体(NIS)介导的碘摄取10, 11。钠碘共转运体(NIS)是一种质膜糖蛋白,属于溶质载体家族5A(slc5a5)12。因此,NIS的充分表达、定位和功能对于RAI治疗至关重要13。在RAI耐药的情况下,NIS的异常表达、定位或功能可能导致RAI无法有效吸收。此外,甲状腺组织中的碘积聚也受到其他甲状腺特异性基因和转录因子的影响,如tsh、tshr、tg、tpo、pbf和pigu,它们共同作用以促进DTC细胞中RAI的积聚。另外,DTC的基因变异,如点突变、基因易位、嵌合融合、基因扩增和缺失,也与RAI耐药相关14。特别是MAPK-PI3K-AKT通路的异常激活,尤其是BRAF V600E和RAS突变,可能导致NIS在细胞膜的异常沉默和内化,从而减弱RAI的疗效15,16。除此之外DTC细胞与肿瘤微环境(TME)之间的相互作用,包括细胞因子、趋化因子、成纤维细胞、脂肪细胞等在这个过程中发挥作用,有可能影响DTC细胞对RAI的敏感性。
总之,RAI耐药机制是一个复杂的过程,涉及到多个分子水平的变化和细胞间的相互作用。对这些机制的深入理解有助于寻找克服RAI耐药的新治疗策略。
靶向治疗药物是克服RAI耐药的策略之一。在RAI敏感的甲状腺癌(DTC)中,包括仑伐替尼、索拉非尼、cabozantinib/ target=_blank class=infotextkey>卡博替尼等多种酪氨酸激酶抑制剂(TKIs)在内的多种分子靶向药物对RAI耐药的DTC具有有效性。

此外,针对MAPK-PI3K-AKT通路的异常激活,尤其是BRAF V600E和RAS突变所导致的NIS在细胞膜的异常沉默和内化,BRAF抑制剂,MEK抑制剂和RET抑制剂等特异性靶向药物可能增强去分化DTC细胞重新摄取放射性碘的能力。
另外,通过抑制NIS的表达和定位,靶向HER2/3、HDAC、EZH2和PPARγ等分子机制可以促使RAI耐药的DTC细胞重新分化。细胞外囊泡(EVs)中含有RAI、NIS和TKIs,可改善药物传递,可能成为提高RAI治疗敏感性的有前景方法。
总之,靶向治疗药物是克服RAI耐药的重要治疗手段。
②特异性靶向药物扭转摄碘能力的现有研究数据
a. 司美替尼增强晚期甲状腺癌放射性碘摄取
2013年一项发表在N Engl J Med的文章公布了一项旨在评估MAPK激酶(MEK)1和MEK2抑制剂司美替尼是否能够逆转对放射性碘的耐药性的研究18。(NCT00970359)
研究首先通过促甲状腺素α刺激的碘-124 PET-CT评估受试者病变的基线碘亲和力。患者随后接受司美替尼治疗,剂量为75 mg,每日2次,口服,治疗4周。在治疗的最后一周,进行第二次促甲状腺素α刺激的124I PET-CT检查。124I剂量预测肿瘤摄取低于2000 cGy的患者终止研究。如果预测病灶内放射性碘的吸收剂量≥2000 cGy,则进行131I全剂量测定,计算可安全给予的最大耐受活度。在用促甲状腺素α进行准备后的下一周,患者接受治疗剂量的放射性碘治疗。司美替尼持续用药至放射性碘治疗后2日。在放射性碘治疗后2个月和6个月评估甲状腺球蛋白水平和影像学反应。

研究筛选的24例患者中,20例可评估。受试者中位年龄61岁(范围,44 ~ 77岁),11例患者为男性。BRAF突变9例,NRAS突变5例。

在20例患者中,司美替尼增加了12例患者(9例BRAF突变患者中的4例和5例NRAS突变患者中的5例)的124I摄取。12例患者中有8例达到了放射性碘治疗的剂量学阈值,包括5例NRAS突变患者。8例接受放射性碘治疗的患者中,5例证实部分缓解,3例疾病稳定。所有患者的血清甲状腺球蛋白水平均降低(平均降幅,89%)。
研究数据验证了司美替尼在对131I放射性碘耐药的一部分甲状腺癌患者中产生了临床上意义重大的碘摄取和保留增加;在携带RAS基因突变疾病的患者中,其效果可能更为显著。
b. 达拉非尼+曲美替尼增强BRAF V 600E突变DTC放射性碘摄取
2023年一项发表在Clinical Cancer Research的文章公布了一项前瞻性多中心、开放标签,达拉非尼-曲美替尼和131I治疗转移性放射性碘难治性BRAF V600E突变分化型甲状腺癌的II期再分化研究19。
试验包括在18个月内RECIST评估进展但无3cm以上病灶的患者。在基线重组人促甲状腺素(rhTSH)刺激诊断性全身扫描(dc1-WBS)后,给予达拉非尼和曲美替尼治疗42天。第二次rhTSH刺激的dc扫描(dc2-WBS)在第28天进行,然后在第35天给予131I(经rhTSH后5.5 GBq–150 mCi)。主要终点是6个月的RECIST客观缓解率。如果在6或12个月时出现部分缓解(PR),可以进行第二个治疗周期。
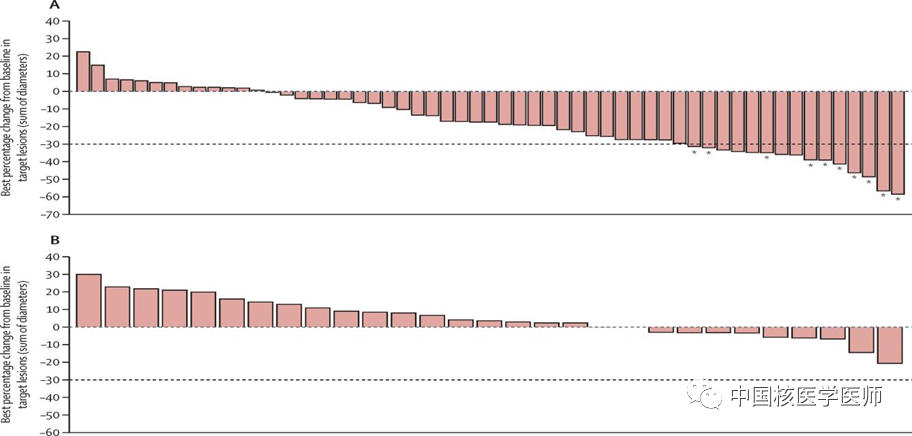
在24例入组患者中,21例在6个月时疗效可评估。结果:dc1-WBS、dc2-WBS和治疗后扫描的异常131I摄取率分别为5%、65%和95%。
在6个月时,38%的患者实现了PR,52%的患者病情稳定,10%的患者病情进展(PD)。10例患者接受了第二个治疗周期:在6个月时观察到一例完全缓解和6例PR。中位无进展生存期(PFS)尚未达到。12个月和24个月的PFS分别为82%和68%。一例患者在24个月时因PD死亡。96%的患者出现了不良事件(AE),其中7例患者出现10个3-4级AE。
达拉非尼-曲美替尼对BRAF V600E突变的DTC患者具有恢复131I摄取的有效性,观察到38%的患者在131I治疗后6个月实现了PR。
相比于特异性靶点的靶向药物,临床上更可及的是抗血管生成的泛靶点靶向药物,这类药物可以使病灶减小,助力放射性碘治疗对于肿瘤负荷较大的患者(肿瘤负荷较大一般被认为是多器官受累,病灶3-5个以上,靶病灶直径总和超过3-4cm)的治疗。
除此之外,临床治疗过程中,病灶摄碘不摄碘并存的发生率高。对于这类病灶,摄碘病灶通过停药准备,TSH升高后用131I治疗效果很好,但是不摄碘病灶在准备的阶段,受TSH的激发,反而有可能出现病灶的生长,而后续131I恰恰对这类病灶不能发挥作用,对于这类病灶的治疗更需要与靶向药物进行联合。
①潜在作用机制
盐酸安罗替尼可以阻断VEGFR1-3,PDGFRα/β,FGFR1-4,c-Kit。与放射性碘治疗联合应用时,安罗替尼可以抑制血管新生,促进血管正常化,抑制肿瘤细胞增殖迁移,增加药物在肿瘤组织分布。除此之外,肿瘤微环境具有缺氧的特点,抗血管生成药物可改善缺氧状态,具有增敏放疗的潜力20,21,22,23。
②泛靶点靶向药物助力131I治疗的现有研究数据
2023年ASCO会议上披露的一项单臂II期开放标签临床试验,研究旨在评估安罗替尼和131I序贯使用对局部晚期或转移性DTC治疗的疗效和安全性24。
研究主要的入选标准包括局部晚期或转移性碘摄取阳性的DTC、ECOG PS为0-1,并且至少有一个可测量的病变。前线使用过酪氨酸激酶抑制剂的患者被排除。患者最初接受安罗替尼(每日12毫克,2周用药/1周停药)进行4个周期的治疗。在第13周开始时,当左旋甲状腺素已停药4周时,进行诊断性131I全身扫描(Dx-WBS),并立即确定具有碘摄取阳性病变的患者进行131I治疗。主要终点是客观缓解率(ORR)。次要终点包括疾病控制率(DCR)、生化缓解率(BRR)、缓解时间(TTR)、无进展生存期(PFS)和安全性。
从2021年6月至2022年12月,共纳入16例局部晚期或转移性DTC患者。在数据截断时,有8例患者(4男性和4女性)因Dx-WBS阴性而退出试验,剩下的8例患者随后接受了131I治疗。完成至少一个周期顺序治疗的6例患者符合数据分析的条件。发现2例患者(33.33%)出现部分缓解,3例患者(50%)出现稳定疾病。达到的ORR为33.33% (95% CI, 4.33-77.72),DCR为83.33% (95% CI, 35.88-99.58),BRR为100% (95% CI, 54.07-100.00),TTR为6.34个月(95% CI, 5.85-NE)。中位PFS尚未达到。6例受试者中有2例(33.33%)出现3级不良事件,其中一例患者因骨转移引起疼痛,另一例患者因药物相关性高血压。
本研究首次展示了安罗替尼和131I序贯治疗的良好疗效和安全性,表明安罗替尼作为局部晚期或转移性DTC碘-131治疗的辅助选择。未来有必要进行关于安罗替尼与碘-131治疗序贯治疗的随机对照研究。
仍有其他一系列同类研究正在进行之中,例如,“安罗替尼联合碘-125粒子植入治疗局部晚期或转移性分化型甲状腺癌的疗效与安全性:一项探索性随机对照、多中心临床研究”、“安罗替尼联合131I治疗晚期转移性分化型甲状腺癌的有效性及安全性临床研究”和“单中心开放标签II期研究,评估仑伐替尼治疗在RAIR甲状腺癌中恢复放射性碘摄取和保留的效果”。期待未来有更多相关研究数据公布,以验证抗血管生成的泛靶点靶向药物与放射性碘治疗联合应用的必要性和安全性。
未来,对于如何更规范临床实践,如何明确肿瘤负荷大的概念,如何明确摄碘不摄碘的界限,以及目前碘131的显像是否能充分真实的评估病灶的摄碘能力等一系列问题,都有待进一步的研究进行探索和明确。
作为甲状腺癌治疗领域探索的新方向,靶向药物与RAI联合治疗展现了一定的治疗潜力。特定靶点的靶向药物在诱导再分化方面治疗取得了一些显著的进展。对于肿瘤负荷较大,摄碘和不摄碘病灶并存的患者,泛靶点的抗血管生成靶向药物在临床上展现出可观的疗效以及助益潜力。
尽管靶向药物与RAI联合治疗呈现出潜在的治疗优势,但仍存在一些挑战。首先,联合治疗可能增加不良反应的风险,需要在治疗效果和安全性之间取得平衡。其次,尽管该研究方向逐渐成为研究关注的重点,但该领域仍需要更多循证医学的数据以及更深入的研究,以探索有效的治疗策略,推动甲状腺癌治疗领域的进一步发展。
综上所述,靶向药物与RAI联合治疗是甲状腺癌治疗的新方向,展现了一定的治疗潜力。随着更多临床研究的进行,相信将为甲状腺癌患者提供更有效的治疗选择。
参考文献
1. Sung H, et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin 2021; 71: 209–49.
2. Pizzato M, et al. The epidemiological landscape of thyroid cancer worldwide: GLOBOCAN estimates for incidence and mortality rates in 2020. Lancet Diabetes Endocrinol 2022; 10: 264–72.
3. LeClair K,et al. Evaluation of gender inequity in thyroid cancer diagnosis: differences by sex in US thyroid cancer incidence compared with a meta-analysis of subclinical thyroid cancer rates at autopsy. JAMA Intern Med 2021; 181: 1351–58.
4. Araque DVP, et al. Thyroid cancer in adolescents and young adults. Future Oncol 2017; 13: 1253–61.
5. Aschebrook-Kilfoy B et al. Thyroid cancer incidence patterns in the United States by histologic type, 1992–2006. Thyroid 2011; 21: 125–34.
6. 晚期甲状腺癌靶向药物应用中国专家共识(2022年版)
7. Brenner H. Long-term survival rates of cancer patients achieved by the end of the 20th century: a period analysis[J]. Lancet, 2002, 360(9340): 1131-1135.
8. Jin Y, et al. Radioiodine refractory differentiated thyroid cancer[J]. Crit Rev Oncol Hematol, 2018, 125(3): 111-120.
9. Durante C, et al. Long-term outcome of 444 patients with distant metastases from papillary and follicular thyroid carcinoma: benefits and limits of radioiodine therapy[J]. J Clin Endocrinol Metab, 2006, 91(8): 2892-2899.
10. Yavuz, et al.. 2022. ‘Iodine-131 Uptake Study’. In StatPearls. Treasure Island (FL): StatPearls Publishing.
11. Koukkou, et al. 2017. Effect of excess iodine intake on thyroid on human health. Minerva Med. 108 (2), 136–146.
12. Aashiq, et al. 2019. Radioiodine-refractory thyroid cancer: molecular basis of redifferentiation therapies, management, and novel therapies. Cancers 11 (9), 1382.
13. Spitzweg, et al. 2002. The sodium iodide symporter: its pathophysiological and therapeutic implications. Clin. Endocrinol. 57 (5), 559–574.
14. Liu Y, et al. Radioiodine therapy in advanced differentiated thyroid cancer: Resistance and overcoming strategy. Drug Resist Updat. 2023 May;68:100939.
15. Durante, et al. 2018. The diagnosis and management of thyroid nodules: a review. JAMA 319 (9), 914–924
16. Oh, et al. 2021. Molecular mechanisms of radioactive iodine refractoriness in differentiated thyroid cancer: impaired sodium iodide symporter (NIS) expression owing to altered signaling pathway activity and intracellular localization of NIS’. Theranostics 11 (13), 6251–6277.
17. Liu Y et al.. Radioiodine therapy in advanced differentiated thyroid cancer: Resistance and overcoming strategy. Drug Resist Updat. 2023 May;68:100939.
18. Ho AL, et al.. Selumetinib-enhanced radioiodine uptake in advanced thyroid cancer. N Engl J Med. 2013 Feb 14;368(7):623-32.
19. Leboulleux S. A Phase II Redifferentiation Trial with Dabrafenib-Trametinib and 131I in Metastatic Radioactive Iodine Refractory BRAF p.V600E-Mutated Differentiated Thyroid Cancer. Clin Cancer Res. 2023 Jul 5;29(13):2401-2409.
20. Lin B, et al. Anlotinib inhibits angiogenesis via suppressing the activation of VEGFR2, PDGFRβ and FGFR1. Gene. 2018 May 15;654:77-86.
21. Su Y et al. Anlotinib Induces a T Cell-Inflamed Tumor Microenvironment by Facilitating Vessel Normalization and Enhances the Efficacy of PD-1 Checkpoint Blockade in Neuroblastoma. Clin Cancer Res. 2022 Feb 15;28(4):793-809.
22. Liang L et al. Autophagy inhibition potentiates the anti-angiogenic property of multikinase inhibitor anlotinib through JAK2/STAT3/VEGFA signaling in non-small cell lung cancer cells. J Exp Clin Cancer Res. 2019 Feb 12;38(1):71.
23. Song F et al. Anlotinib suppresses tumor progression via blocking the VEGFR2/PI3K/AKT cascade in intrahepatic cholangiocarcinoma. Cell Death Dis. 2020 Jul 24;11(7):573.
24. Abstract No. e18102, Publication Only, 2023 ASCO